Древнегреческие мудрецы первыми сказали слово "элемент", и произошло это за пять веков до нашей эры. Правда, "элементами" у древних греков считались земля, вода, воздух и огонь, а вовсе не железо, кислород, водород, азот и другие элементы теперешних химиков.
В средние века ученые знали уже десять химических элементов - семь металлов (золото, серебро, медь, железо, олово, свинец и ртуть) и три неметалла (серу, углерод и сурьму).
Смотреть что такое "ртуть" в других словарях
Самый твердый материал в организме человека - зубная эмаль. Это должно быть трудно, так что наши зубы могут служить нам на всю жизнь кусать и жевать; однако, как бы то ни было, зубная эмаль восприимчива к химическим атакам. Кислоты, обнаруженные в некоторых продуктах или сделанные бактериями, которые питаются остатками пищи на наших зубах, способны растворять эмаль. Незащищенный эмалью, зуб начнет распадаться, тем самым развивая полости и другие стоматологические проблемы.
После нескольких лет исследований было обнаружено, что избыточные соединения фтора в питьевой воде являются причиной обоих этих эффектов. Защитные эффекты фтора имеют простое химическое объяснение. Зубная эмаль состоит в основном из минерала, называемого гидроксиапатитом, который состоит из кальция, фосфора, кислорода и водорода. Теперь мы знаем, что фтор сочетается с гидроксиапатитом для получения фторапатита, который более устойчив к кислотному распаду, чем гидроксиапатит. Это преднамеренное фторирование в сочетании с использованием фторидсодержащих зубных паст и улучшенной гигиеной полости рта привело к уменьшению кариеса на 60% у детей.
Алхимики очень долго обходились без химических формул
. В употреблении были странные значки, причем почти каждый химик пользовался своей собственной системой обозначений веществ. А описания химических превращений походили на сказки и легенды.
Вот как, например, излагали алхимики реакцию оксида ртути (вещества красного цвета) с соляной (хлороводородной) кислотой:
Общенациональное сокращение кариеса было названо важным достижением общественного здравоохранения в истории. Так же, как язык имеет алфавит, из которого строятся слова, химия имеет алфавит, из которого описана материя. Однако химический алфавит больше, чем тот, который мы используем для написания. Возможно, вы уже поняли, что химический алфавит состоит из химических элементов. Их роль играет центральную роль в химии, поскольку они объединяются в миллионы и миллионы известных соединений.
Элемент является основным химическим строительным блоком материи; это самое простое химическое вещество. Химические символы полезны для кратковременного представления элементов, присутствующих в веществе.
- Определите химический элемент и укажите примеры обилия различных элементов.
- Представляют химический элемент с химическим символом.
- Натрий ртутный фосфор калий йод.
- Какой элемент представлен каждым химическим символом?
- Приведите несколько примеров того, как изменяется количество элементов.
- Почему химические символы так полезны?
- Каков источник письма для химического символа?
- Элементы варьируются от небольшого процента до более чем 30% атомов вокруг нас.
- Буквы обычно исходят от имени элемента.
- Вся материя состоит из элементов.
- Химические элементы представлены одно - или двухбуквенным символом.
- Натрий вода сжиженный азот.
"Являлся красный лев - и был он женихом,
И в теплой жидкости они его венчали
С прекрасной лилией, и грели их огнем,
И из сосуда их в сосуд перемещали..."
(И. В. Гёте, "Фауст")
Алхимики считали, что химические элементы связаны со звездами и планетами и присваивали им астрологические символы. Золото называлось Солнцем, а обозначалось кружком с точкой; медь - Венерой, символом этого металла служило "венерино зеркальце", а железо - Марсом; как и полагается богу войны, обозначение этого металла включало щит и копье:
Бумага из углеродистого бетона. . Напишите химический символ для каждого элемента. Элемент не элемент, а не элемент, а не элемент. . По соглашению вторая буква в символе элемента всегда имеет строчные значения.
- Объясните, как все вещество состоит из атомов.
- Описать современную атомную теорию.
Должно быть очевидно, что куски все еще алюминиевой фольги; они просто становятся все меньше и меньше. Но как далеко вы можете выполнить это упражнение, по крайней мере теоретически? Можете ли вы продолжить нарезку алюминиевой фольги на половинки навсегда, делая меньшие и мелкие кусочки? Или есть какой-то предел, какой-то абсолютный наименьший кусок алюминиевой фольги?
В XVIII веке укоренилась система обозначений элементов (которых в то время стало известно уже три десятка) в виде геометрических фигур - кружков, полуокружностей, треугольников, квадратов. Этот способ изображения химических веществ придумал английский ученый, физик и химик Джон Дальтон.
Однако различать химические символы разных элементов в книгах и научных журналах было довольно трудно. А каково было работать наборщикам в тогдашних типографиях! Как им было отличить знак водорода, который представлял собой три концентрических окружности, нарисованных сплошной линией, и с точкой в центре, от знака кислорода - тоже трех концентрических окружностей, одна из которых пунктирная, и без точки?
Вот символы кислорода, серы, водорода и азота, которые использовал Дальтон:
Карьерный фокус: клинический химик
Рисунок 11 Тенденции на периодической таблице.
Относительные размеры атомов показывают несколько тенденций в отношении структуры периодической таблицы. Атомы становятся более крупными вниз по столбцу и меньше проходят через период. Клиническая химия - это область химии, связанная с анализом жидкостей организма для определения состояния здоровья организма человека. Клинические химики измеряют различные вещества , начиная от простых элементов, таких как натрий и калий, до сложных молекул, таких как белки и ферменты, в крови, моче и других биологических жидкостях.
 Наконец, в 1814 году появились символы и названия химических элементов, которыми химики пользуются по сей день. Шведский химик Йёнс-Якоб Берцелиус предложил обозначать химические элементы первой буквой (или первой и одной из следующих букв) латинского названия элемента.
Наконец, в 1814 году появились символы и названия химических элементов, которыми химики пользуются по сей день. Шведский химик Йёнс-Якоб Берцелиус предложил обозначать химические элементы первой буквой (или первой и одной из следующих букв) латинского названия элемента.
Например, водород
(по-латыни "гидрогениум", Hydrogenium
) - Н (читается "аш"), углерод
(по-латыни "карбонеум", Carboneum
) - C, (по-латыни "аурум", Aurum
) - Au (читается тоже "аурум").
Отсутствие или наличие или аномально низкие или большие количества вещества могут быть признаком какого-либо заболевания или признака здоровья. Многие клинические химики используют сложную технику и сложные химические реакции в своей работе, поэтому им нужно не только понимать основную химию, но и быть знакомыми со специальными инструментами и как интерпретировать результаты испытаний.
Элементы организованы по атомному номеру. в левой трех четверти периодической таблицы правый квартал периодической таблицы следующий-последний столбец периодической таблицы - средняя часть периодической таблицы. Когда вы переходите через периодическую таблицу, атомные радиусы уменьшаются; по мере того как вы спускаетесь по периодической таблице, атомные радиусы возрастают.
Русские названия многих элементов звучат совсем иначе, чем латинские, но что поделаешь - химические символы проходится заучивать наизусть, как заучивают латинские термины студенты-медики, будущие врачи.
Совершенно ясно, что запомнить сразу все символы и названия элементов (а их сейчас известно 114) - задача непосильная. Поэтому для начала можно ограничиться самыми распространенными:
Некоторые характеристики элементов связаны с их положением на периодической таблице. Какие элементы имеют химические свойства, аналогичные свойствам магния? натрий фтор кальций барий селен. Химические элементы расположены на диаграмме, называемой периодической таблицей. . Какие элементы имеют химические свойства, аналогичные свойствам лития?
Натрий кальций бериллий барий калий. . Какие элементы имеют химические свойства, аналогичные свойствам хлора? Чтобы вы поняли материал в этой главе, вы должны просмотреть значения следующих жирных терминов и спросить себя, как они относятся к темам в этой главе.
| Русское название | Химический символ и атомный номер элемента | Латинское название |
Произношение символа |
| Азот | 7 N | Nitrogenium | эн |
| Алюминий | 13 Al | Aluminium | алюминий |
| Бром | 35 Br | Bromum | бром |
| Водород | 1 H | Hydrogenium | аш |
| Гелий | 2 He | Helium | гелий |
| Железо | 26 Fe | Ferrum | феррум |
| Золото | 79 Au | Aurum | аурум |
| Иод | 53 I | Iodum | иод |
| Калий | 19 K | Kalium | калий |
| Кальций | 20 Ca | Calcium | кальций |
| Кислород | 8 O | Oxygenium | о |
| Кремний | 14 Si | Silicium | силициум |
| Магний | 12 Mg | Magnesium | магний |
| Медь | 29 Cu | Cuprum | купрум |
| Натрий | 11 Na | Natrium | натрий |
| Олово | 50 Sn | Stannum | станнум |
| Свинец | 82 Pb | Plumbum | плюмбум |
| Сера | 16 S | Sulfur | эс |
| Серебро | 47 Ag | Argentum | аргентум |
| Углерод | 6 C | Carboneum | це |
| Фосфор | 15 P | Phosphorus | пэ |
| Фтор | 9 F | Fluorum | фтор |
| Хлор | 17 Cl | Chlorum | хлор |
| Хром | 24 Cr | Chromium | хром |
| Цинк | 30 Zn | Zincum | цинк |
Названия и символы химических элементов
§ 4. Химические знаки и формулы
К символьным моделям в химии относят знаки или символы химических элементов, формулы веществ и уравнения химических реакций, которые лежат в основе «химической письменности». Ее основоположником является шведский химик Йенс Якоб Берцелиус. Письменность Берцелиуса строится на важнейшем из химических понятий – «химический элемент». Химическим элементом называют вид одинаковых атомов.
Элемент - это вещество, которое нельзя разбить на более простые химические вещества. Известно только около 90 естественных элементов. Они имеют различное изобилие на Земле и в теле. Каждый элемент имеет одно - или двухбуквенный химический символ. Современная атомная теория утверждает, что наименьшая часть элемента является атомом. Отдельные атомы чрезвычайно малы, порядка 10 -10 м в поперечнике. Большинство элементов существуют в чистом виде как отдельные атомы, но некоторые существуют как двухатомные молекулы.
Сами атомы состоят из субатомных частиц. Электрон представляет собой крошечную субатомную частицу с отрицательным зарядом. Протон имеет положительный заряд и, хотя и мал, намного больше электрона. Нейтрон также намного больше, чем электрон, но не имеет электрического заряда.
Берцелиус предложил обозначать химические элементы первой буквой их латинских названий. Так символом кислорода стала первая буква его латинского названия: кислород – О (читается «о», т.к. латинское название этого элемента oxygenium ). Соответственно водород получил символ H (читается «аш», т.к. латинское название этого элемента hydrogenium ), углерод – С (читается «цэ», т.к. латинское название этого элемента carboneum ). Однако латинские названия хрома (chromium ), хлора (chlorum ) и меди (cuprum ) так же, как и углерода, начинаются на «С». Как же быть? Берцелиус предложил гениальное решение: такие символы записывать первой и одной из последующих букв, чаще всего второй. Так, хром обозначается Сr (читается «хром»), хлор – Cl (читается «хлор»), медь – Cu (читается «купрум»).
Протоны, нейтроны и электроны имеют специфическое расположение в атоме. Протон и нейтроны находятся в центре атома, сгруппированные в ядро. Электроны находятся в нечетких облаках вокруг ядра. Каждый элемент имеет характеристическое число протонов в своем ядре. Это число протонов является атомным номером элемента. Элемент может иметь различное количество нейтронов в ядрах его атомов; такие атомы называются изотопами. Два изотопа водорода являются дейтерием, с протоном и нейтроном в его ядре и тритием с протоном и двумя нейтронами в его ядре.
Русские и латинские названия, знаки 20 химических элементов и их произношения приведены в табл. 2.
В нашей таблице уместилось всего 20 элементов. Чтобы увидеть все 110 элементов, известных на сегодняшний день, нужно посмотреть в таблицу химических элементов Д.И.Менделеева.
Таблица 2
Названия и символы некоторых химических элементов
|
Русское название Сумма чисел протонов и нейтронов в ядре называется массовым числом и используется для выделения изотопов друг от друга. Массы отдельных атомов измеряются в единицах атомной массы. Поскольку разные изотопы элемента имеют разные массы, атомная масса элемента является средневзвешенной массой всех естественных изотопов элемента. Современная теория поведения электронов называется квантовой механикой. Согласно этой теории, электроны в атомах могут иметь только конкретные или квантованные энергии. Электроны сгруппированы в общие области , называемые оболочками, а внутри них - в более конкретные области, называемые подоболочками. Существует четыре типа подоболочек, и каждый тип может удерживать до максимального количества электронов. Распределение электронов в оболочки и подоболочки - это электронная конфигурация атома. Химия обычно возникает из-за взаимодействия между электронами самой внешней оболочки разных атомов, называемой электронами валентной оболочки. |
Химический знак |
Произношение |
Латинское название |
|
Алюминий Электроны во внутренних оболочках называются электронами ядра. Элементы сгруппированы по сходным химическим свойствам в диаграмму, называемую периодической таблицей. Вертикальные столбцы элементов называются группами или семействами. Некоторые из групп элементов имеют названия, такие как щелочные металлы, щелочноземельные металлы, галогены и благородные газы. Горизонтальный ряд элементов называется периодом. Периоды и группы имеют различное количество элементов в них. Периодическая таблица разделяет элементы на металлы, неметаллы и полуметаллы. |
Алюминий |
||
|
Гидраргирум Периодическая таблица также разделяется на основные элементы группы, переходные металлы, элементы лантанидов и актинидные элементы. Элементы лантаноидов и актинидов также упоминаются как элементы внутреннего переходного металла. Форма периодической таблицы отражает последовательное заполнение оболочек и подоболочек в атомах. Периодическая таблица помогает нам понять тенденции в некоторых свойствах атомов. Одним из таких свойств является атомный радиус атомов. Сверху донизу периодической таблицы атомы становятся больше, потому что электроны занимают большие и большие оболочки. Слева направо через периодическую таблицу электроны заполняют одну и ту же оболочку, но притягиваются увеличивающимся положительным зарядом от ядра, и, следовательно, атомы становятся меньше. |
|||
|
Аргентум |
|||
Чаще всего в состав веществ входят атомы нескольких химических элементов. Изобразить мельчайшую частицу вещества, например молекулу, можно с помощью моделей-шариков так, как вы это делали на предыдущем уроке. На рис. 33 изображены объемные модели молекул воды (а) , сернистого газа (б) , метана (в) и углекислого газа (г) .
Какова масса электрона в единицах атомной массы? В сноске в этой главе альфа-частица была определена как частица с 2 протонами и 2 нейтронами. Какова масса в граммах альфа-частицы? Какова атомная масса мифического мира? Поскольку распределение изотопов различно на разных планетах в солнечной системе, средняя атомная масса любого элемента отличается от планеты к планете. Какова атомная масса водорода на Меркурий? Что еще есть химические элементы?
И хотя ответ на этот вопрос был прост для провозглашения, вопросы возникают еще более интересными: можем ли мы обнаружить или создать бесконечное количество химических элементов?, Для чего они будут служить нам? Как выбираются их имена и символы? химические вещества?
Чаще для обозначения веществ химики пользуются не материальными моделями, а знаковыми. С помощью символов химических элементов и индексов записываются формулы веществ. Индекс показывает, сколько атомов данного элемента входит в состав молекулы вещества. Он записывается внизу справа от знака химического элемента . Например, формулы упомянутых выше веществ записывают так: Н 2 О, SO 2 , CH 4 , CO 2 .
Химическая формула – основная знаковая модель в нашей науке. Она несет очень важную для химика информацию. Химическая формула показывает: конкретное вещество; одну частицу этого вещества, например одну молекулу; качественный состав вещества, т.е. атомы каких элементов входят в состав данного вещества; количественный состав , т.е. сколько атомов каждого элемента входит в состав молекулы вещества.
По формуле вещества можно определить также, простое оно или сложное.
Простыми веществами называют вещества, состоящие из атомов одного элемента. Сложные вещества образованы атомами двух или более различных элементов.
Например, водород Н 2 , железо Fe, кислород О 2 – простые вещества , а вода Н 2 О, углекислый газ СО 2 и серная кислота H 2 SO 4 – сложные.
1. Знаки каких химических элементов содержат заглавную букву С? Запишите их и произнесите.
2. Из табл. 2 выпишите отдельно знаки элементов-металлов и элементов-неметаллов. Произнесите их названия.
3. Что такое химическая формула ? Запишите формулы следующих веществ:
а) серной кислоты, если известно, что в состав ее молекулы входят два атома водорода, один атом серы и четыре атома кислорода;
б) сероводорода, молекула которого состоит из двух атомов водорода и одного атома серы;
в) сернистого газа, молекула которого содержит один атом серы и два атома кислорода.
4. Что объединяет все эти вещества?
Изготовьте из пластилина объемные модели молекул следующих веществ:
а) аммиака, молекула которого содержит один атом азота и три атома водорода;
б) хлороводорода, молекула которого состоит из одного атома водорода и одного атома хлора;
в) хлора, молекула которого состоит из двух атомов хлора.
Напишите формулы этих веществ и прочитайте их.
5. Приведите примеры превращений, когда известковая вода является определяемым веществом, а когда – реактивом.
6. Проведите домашний эксперимент по определению крахмала в продуктах питания. Какой реактив вы использовали при этом?
7. На рис. 33 изображены модели молекул четырех химических веществ. Сколько химических элементов образуют эти вещества? Запишите их символы и произнесите их названия.
8. Возьмите пластилин четырех цветов. Скатайте самые маленькие шарики белого цвета – это модели атомов водорода, синие шарики побольше – модели атомов кислорода, черные шарики – модели атомов углерода и, наконец, самые большие шарики желтого цвета – модели атомов серы. (Конечно, цвет атомов мы выбрали условно, для наглядности.) С помощью шариков-атомов изготовьте объемные модели молекул, показанных на рис. 33.
; 2) 9-й класс . Первая часть курса ... с высокого старта с опорой...
Основная образовательная программа начального общего образования Муниципального бюджетного общеобразовательного учреждения «Средняя общеобразовательная школа №7»
Основная образовательная программа... : физики, химии , биологии, географии... старта , с 6,2-6,0 6,7-6,3 7,2-7,0 6,3-6,1 6,9-6,5 7,2-7,0 Бег 1000 м Без учета времени 2 КЛАСС ... Программа курса английского языка к УМК «Enjoy English» для учащихся 2 – 9 классов общеобразовательных учреждений . ...
Публичный отчет государственного бюджетного общеобразовательного учреждения Самарской области (1)
Публичный отчет... . Химия 8-11класс. Программа курса химии для 8-11 классов общеобразовательных учреждений ./автор Е.Е.Минченков,Т.В.Смирнова, Л.А.Цветков. М.: Дрофа,2008г. Химия .Учебник 8 класса ... , походы на природу, «Веселые старты », спортивные игры на воздухе, что...
Методические рекомендации к курсу "Математика. 2 класс"/ Аргинская И. И., Кормишина С. Н самара: Издательство "Учебная литература": Издательский дом "Федоров", 2012. 336 с (Программы и планирование) Экземпляры: всего: 2 сош3(2)
Методические рекомендацииРекомендации к рабочей тетради "Школьный старт ". Педагогическая диагностика стартовой готовности к... А.О. Сороко-Цюпы. 27. Габриелян О.С. Программа курса химии для 8-11 классов общеобразовательных учреждений / Габриелян О.С.. - М.: Дрофа, 2011. ...
См. также: Список химических элементов по атомным номерам и Алфавитный список химических элементов Содержание 1 Символы, используемые в данный момент … Википедия
См. также: Список химических элементов по символам и Алфавитный список химических элементов Это список химических элементов, упорядоченный в порядке возрастания атомных номеров. В таблице приводятся название элемента, символ, группа и период в… … Википедия
- (ИСО 4217) Коды для представления валют и фондов Codes for the representation of currencies and funds (англ.) Codes pour la représentation des monnaies et types de fonds (фр.) … Википедия
Простейшая форма материи, которая может быть идентифицирована химическими методами. Это составные части простых и сложных веществ, представляющие собой совокупность атомов с одинаковым зарядом ядра. Заряд ядра атома определяется числом протонов в … Энциклопедия Кольера
Содержание 1 Эпоха палеолита 2 10 е тысячелетие до н. э. 3 9 е тысячелетие до н. э … Википедия
Содержание 1 Эпоха палеолита 2 10 е тысячелетие до н. э. 3 9 е тысячелетие до н. э … Википедия
У этого термина существуют и другие значения, см. Русские (значения). Русские … Википедия
Терминология 1: : dw Номер дня недели. «1» соответствует понедельнику Определения термина из разных документов: dw DUT Разность между московским и всемирным координированным временем, выраженная целым количеством часов Определения термина из… … Словарь-справочник терминов нормативно-технической документации
Как пользоваться таблицей Менделеева? Для непосвященного человека читать таблицу Менделеева – всё равно, что для гнома смотреть на древние руны эльфов. А таблица Менделеева может рассказать о мире очень многое.
Помимо того, что сослужит вам службу на экзамене, она еще и просто незаменима при решении огромного количества химических и физических задач. Но как ее читать? К счастью, сегодня этому искусству может научиться каждый. В этой статье расскажем, как понять таблицу Менделеева.
Периодическая система химических элементов (таблица Менделеева) – это классификация химических элементов, которая устанавливает зависимость различных свойств элементов от заряда атомного ядра.
История создания Таблицы
Дмитрий Иванович Менделеев был не простым химиком, если кто-то так думает. Это был химик, физик, геолог, метролог, эколог, экономист, нефтяник, воздухоплаватель, приборостроитель и педагог. За свою жизнь ученый успел провести фундаментально много исследований в самых разных областях знаний. Например, широко распространено мнение, что именно Менделеев вычислил идеальную крепость водки – 40 градусов.
Не знаем, как Менделеев относился к водке, но точно известно, что его диссертация на тему «Рассуждение о соединении спирта с водой» не имела к водке никакого отношения и рассматривала концентрации спирта от 70 градусов. При всех заслугах ученого, открытие периодического закона химических элементов – одного их фундаментальных законов природы, принесло ему самую широкую известность.

Существует легенда, согласно которой периодическая система приснилась ученому, после чего ему осталось лишь доработать явившуюся идею. Но, если бы все было так просто.. Данная версия о создании таблицы Менделеева, по-видимому, не более чем легенда. На вопрос о том, как была открыта таблица, сам Дмитрий Иванович отвечал: «Я над ней, может быть, двадцать лет думал, а вы думаете: сидел и вдруг… готово»
В середине девятнадцатого века попытки упорядочить известные химические элементы (известно было 63 элемента) параллельно предпринимались несколькими учеными. Например, в 1862 году Александр Эмиль Шанкуртуа разместил элементы вдоль винтовой линии и отметил циклическое повторение химических свойств.
Химик и музыкант Джон Александр Ньюлендс предложил свой вариант периодической таблицы в 1866 году. Интересен тот факт, что в расположении элементов ученый пытался обнаружить некую мистическую музыкальную гармонию. В числе прочих попыток была и попытка Менделеева, которая увенчалась успехом.

В 1869 году была опубликована первая схема таблицы, а день 1 марта 1869 года считается днем открытия периодического закона. Суть открытия Менделеева состояла в том, что свойства элементов с ростом атомной массы изменяются не монотонно, а периодически.
Первый вариант таблицы содержал всего 63 элемента, но Менделеев предпринял ряд очень нестандартных решений. Так, он догадался оставлять в таблице место для еще неоткрытых элементов, а также изменил атомные массы некоторых элементов. Принципиальная правильность закона, выведенного Менделеевым, подтвердилась очень скоро, после открытия галлия, скандия и германия, существование которых было предсказано ученым.
Современный вид таблицы Менделеева
Ниже приведем саму таблицу
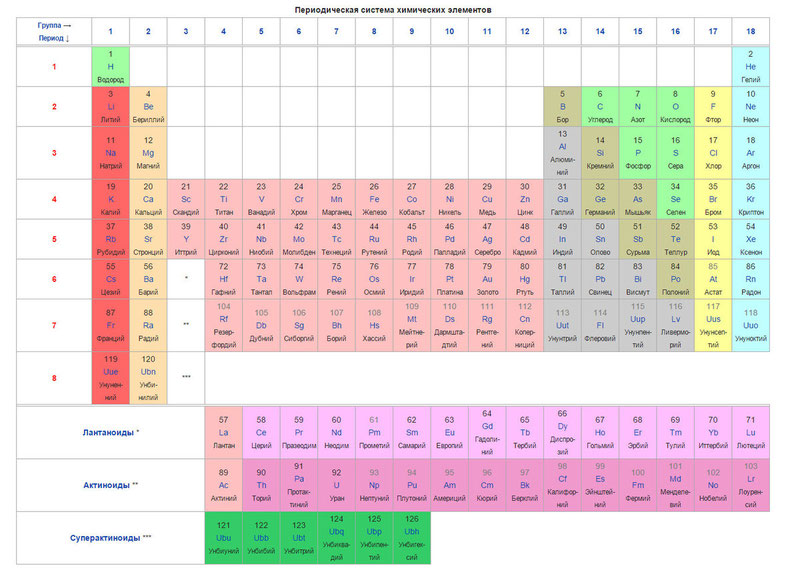
Сегодня для упорядочения элементов вместо атомного веса (атомной массы) используется понятие атомного числа (числа протонов в ядре). В таблице содержится 120 элементов, которые расположены слева направо в порядке возрастания атомного числа (числа протонов)
Столбцы таблицы представляют собой так называемые группы, а строки – периоды. В таблице 18 групп и 8 периодов.
- Металлические свойства элементов при движении вдоль периода слева направо уменьшаются, а в обратном направлении – увеличиваются.
- Размеры атомов при перемещении слева направо вдоль периодов уменьшаются.
- При движении сверху вниз по группе увеличиваются восстановительные металлические свойства.
- Окислительные и неметаллические свойства при движении вдоль периода слева направо увеличиваются.
Что мы узнаем об элементе по таблице? Для примера, возьмем третий элемент в таблице – литий, и рассмотрим его подробно.

Первым делом мы видим сам символ элемента и его название под ним. В верхнем левом углу находится атомный номер элемента, в порядке которого элемент расположен в таблице. Атомный номер, как уже было сказано, равен числу протонов в ядре. Число положительных протонов, как правило, равно числу отрицательных электронов в атоме (за исключением изотопов).
Атомная масса указана под атомным числом (в данном варианте таблицы). Если округлить атомную массу до ближайшего целого, мы получим так называемое массовое число. Разность массового числа и атомного числа дает количество нейтронов в ядре. Так, число нейтронов в ядре гелия равно двум, а у лития – четырем.
Вот и закончился наш курс "Таблица Менделеева для чайников". В завершение, предлагаем вам посмотреть тематическое видео, и надеемся, что вопрос о том, как пользоваться периодической таблицей Менделеева, стал вам более понятен. Напоминаем, что изучать новый предмет всегда эффективнее не одному, а при помощи опытного наставника. Именно поэтому, никогда не стоит забывать о студенческом сервисе , который с радостью поделится с вами своими знаниями и опытом.
Инструкция
Периодическая система представляет собой многоэтажный «дом», в котором располагается большое количество квартир. Каждый «жилец» или в своей собственной квартире под определенным номером, который является постоянным. Помимо этого элемент имеет «фамилию» или название, например кислород, бор или азот. Кроме этих данных в каждой «квартире» или указана такая информация, как относительная атомная масса, которая может иметь точные или округленные значения.
Как в любом доме, здесь имеются «подъезды», а именно группы. Причем в группах элементы располагаются слева и справа, образуя . В зависимости от того, с какой стороны их больше, та называется главной. Другая подгруппа, соответственно, будет побочной. Также в таблице имеются «этажи» или периоды. Причем периоды могут быть как большими (состоят из двух рядов) так и малыми (имеют только один ряд).
По таблице можно показать строение атома элемента, каждый из которых имеет положительно заряженное ядро, состоящее из протонов и нейтронов, а также вращающихся вокруг него отрицательно заряженных электронов. Число протонов и электронов численно совпадает и определяется в таблице по порядковому номеру элемента. Например, химический элемент сера имеет №16, следовательно, будет иметь 16 протонов и 16 электронов.
Чтобы определить количество нейтронов (нейтральных частиц, также расположенных в ядре) вычтите из относительной атомной массы элемента его порядковый номер. Например, железо имеет относительную атомную массу равную 56 и порядковый номер 26. Следовательно, 56 – 26 = 30 протонов у железа.
Электроны находятся на разном расстоянии от ядра, образуя электронные уровни. Чтобы определить число электронных (или энергетических) уровней, нужно посмотреть на номер периода, в котором располагается элемент. Например, алюминий находится в 3 периоде, следовательно, у него будет 3 уровня.
По номеру группы (но только для главной подгруппы) можно определить высшую валентность. Например, элементы первой группы главной подгруппы (литий, натрий, калий и т.д.) имеют валентность 1. Соответственно, элементы второй группы (бериллий, магний, кальций и т.д.) будут иметь валентность равную 2.
Также по таблице можно проанализировать свойства элементов. Слева направо металлические свойства ослабевают, а неметаллические усиливаются. Это хорошо видно на примере 2 периода: начинается щелочным металлом натрием, затем щелочноземельный металл магний, после него амфотерный элемент алюминий, затем неметаллы кремний, фосфор, сера и заканчивается период газообразными веществами – хлором и аргоном. В следующем периоде наблюдается аналогичная зависимость.
Сверху вниз также наблюдается закономерность – металлические свойства усиливаются, а неметаллические ослабевают. То есть, например, цезий гораздо активнее по сравнению с натрием.
Все названия химических элементов происходят из латинского языка. Это необходимо в первую очередь для того, чтобы ученые разных стран могли понимать друг друга.
Химические знаки элементов
Элементы принято обозначать химическими знаками (символами). По предложению шведского химика Берцелиуса (1813 г.) химические элементы обозначают начальной или начальной и одной из последующих букв латинского названия данного элемента; первая буква всегда прописная, вторая строчная. Например, водород (Hydrogenium) обозначается буквой H, кислород (Oxygenium) – буквой O, сера (Sulfur) – буквой S; ртуть (Hydrargyrum) – буквами Hg, алюминий (Aluminium) – Al, железо (Ferrum) – Fe и т. д.

Рис. 1. Таблица химических элементов с названиями на латинском и русском языке.
Русские названия химических элементов зачастую представляют собой латинские названия с видоизмененными окончаниями. Но также существует множество элементов, произношение которых отличается от латинского первоисточника. Это либо коренные русские слова (например, железо), либо слова, которые являются переводом (пример – кислород).
Химическая номенклатура
Химическая номенклатура – правильное наименование химических веществ. Латинское слово nomenclatura переводится как «перечень имен, названий»
На ранней стадии развития химии веществам давались произвольные, случайные наименования (тривиальные названия). Легколетучие жидкости назывались спиртами, к ним относились «соляной спирт» – водный раствор соляной кислоты, «силитряный спирт» – азотная кислота, «нашатырный спирт» – водный раствор аммиака. Маслообразные жидкости и твердые вещества назывались маслами, например, концентрированная серная кислота носила название «купоросное масло», хлорид мышьяка – «мышьяковое масло».
Иногда вещества получали название по имени его первооткрывателя, например, «глауберова соль» Na 2 SO 4 *10H 2 O, открытая немецким химиком И. Р. Глаубером в XVII веке.

Рис. 2. Портрет И. Р. Глаубер.
В старинных названиях могли указываться вкус веществ, цвет, запах, внешний вид, медицинское действие. Одно вещество иногда имело несколько наименований.
К концу XVIII века химикам было известно не более 150-200 соединений.
Первую систему научных названий в химии выработала в 1787 г. комиссия химиков во главе с А. Лавуазье. Химическая номенклатура Лавуазье послужила основой для создания национальных химических номенклатур. Для того, чтобы химики разных стран понимали друг друга, номенклатура должна быть единой. В настоящее время построение химических формул и названий неорганических веществ подчиняется системе номенклатурных правил, созданной комиссией Международного союза теоретической и прикладной химии (ИЮПАК). Каждое вещество изображается формулой, в соответствии с ней строится систематическое название соединения.

Рис. 3. А. Лавуазье.
Что мы узнали?
Все химические элементы имеют латинские корни. Латинские названия химических элементов являются общепринятыми. В русский язык они переносятся с помощью калькирования или перевода. однако некоторые слова имеют изначально русское значение, например, медь или железо. Химической номенклатуре подчиняются все химические вещества, состоящие из атомов и молекул. впервые система научных названий была разработана А. Лавуазье.
Тест по теме
Оценка доклада
Средняя оценка: 4.2 . Всего получено оценок: 768.